Química orgánica
1.- Definición:
Llamada también “Química de los compuestos del Carbono”.
Es la rama de la química, que estudia la estructura y propiedades de los compuestos del carbono que constituyen principalmente la materia viva, su aplicación a la industria y al desarrollo tecnológico.
Los “padres de la química” son Friedrich Kekulé y Archibald Scott Couper.
http://es.wikipedia.org/wiki/Qu%C3%ADmica_org%C3%A1nica
http://www.visionlearning.com/library/modulo_espanol.php?mid=60&l=s&c3=
1.2.- La importancia de la química orgánica:
La química orgánica es importante porque nosotros estamos formados por moléculas orgánicas, proteínas ácidos nucleicos, azúcares y grasas. Todos los que nombre anteriormente son compuestos cuya base principal es el carbono.
http://www.quimicaorganica.net/
2.- Estudio del átomo de carbono:
Presenta una importante capacidad de combinación debido a su configuración electrónica. Estos átomos pueden unirse entre sí formando estructuras muy complejas y enlazarse a otros átomos. La enorme diversidad en los compuestos de carbono, hace de su estudio químico una importante área de conocimiento puro.
2.1.- Propiedades físicas
Este elemento se puede encontrar en dos formas:
- Es buen conductor de electricidad y tiene un brillo metálico
- Es usado como electrodos inertes en pilas o celdas galvánicas.
- Es usado para cortar metales en la cuchilla de los tornos, taladros, etc.
- Los diamantes transparentes son utilizados como piedras preciosas de gran valor monetario y no sirve para conducir electricidad.
2.2.- Propiedades químicas: explicación y gráfico de cada uno.
Esta propiedad consiste en que los cuatro orbitales híbridos son de igual intensidad de energía y por lo tanto sus cuatro enlaces del carbono son iguales y de igual clase. Esto significa que el carbono ejerce la misma fuerza de unión por sus cuatro enlaces.
Ejemplo
- En el metano los cuatro hidrógenos son atraídos por el carbono con la misma fuerza ya que sus cuatro enlaces son de la misma clase.

El carbono se manifiesta siempre como tetravalente y sus enlaces son covalentes e iguales entre si.
El carbono en el estado basal tiene dos electrones en el subnivel 2s y dos electrones en el subnivel 2p.
De acuerdo a la configuración electróni ca que describimos deberíamos esperar que el carbono se comporte como divalente puesto que tiene 2 orbitales o electrones sin aparear.
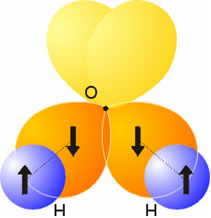
Es la función de orbitales de diferentes energías del mismo nivel pero de diferente subnivel, resultando orbitales de energía constante y de igual forma
Ejemplo:
- La configuración electrónica del boro: esto se debe a sus conglomerados atómicos se tienden a excitarse, produciendo el fenómeno de hibridación.
Al compartir sus electrones con otros átomos de carbono puede originar enlaces simples, dobles, o triples de tal manera que cada enlace representa un par covalente y comparten dos y tres pares de electrones.
http://ar.answers.yahoo.com/question/index?qid=20070501162406AA2Q7mf
3.- Funciones químicas orgánicas.
3.1: Definición:
Conjunto de propiedades y comportamientos comunes a una serie de compuestos análogos.
3.2.- Principales funciones químicas orgánicas
No hay comentarios:
Publicar un comentario